1.1 MODE OPERATOIRE:
Schťma:
NOTE D'INTRODUCTION :
La dťmarche "Bidon Futť" permet certes de contribuer ŗ la
prťservation de l'environnement en collectant les effluents de travaux pratiques au lieu
de les rejeter ŗ l'ťvier, mais peut aussi permettre de sensibiliser les ťlŤves au
"comment" du traitement des dťchets chimiques et au devenir de ceux-ci aprŤs
traitement.
On pourrait ainsi ťviter que les "bidons futťs" ne deviennent une sorte de
"boÓtes noires", ťquivalents pťdagogiques du siphon de l'ťvier...
Le T.P. proposť ici permet de concrťtiser jusqu'ŗ son terme ultime la dťmarche
"Bidon Futť" de tri sťlectif des dťchets chimiques, telle qu'elle a ťtť
mise en place au Lycťe Louis Vincent de Metz, en faisant appel aux compťtences acquises
en classe de seconde.
Il peut faire suite ŗ la visite du pilote de traitement des dťchets chimiques situť
dans le laboratoire de Gťnie Chimique du Lycťe ou ŗ une dťmonstration rťalisťe en
classe ŗ l'aide du mini-pilote didactique rťalisť par le Lycťe (renseignements
disponibles sur demande).
Place dans la progression:
Cette sťance de travaux pratique pourrait idťalement prendre place en
fin de premier trimestre, une fois achevťe la premiŤre partie "Chimie des champs et
des jardins" (dont il reprend de nombreuses notions en prť-requis) et aprŤs le T.P.
sur la notion d'ťlťment chimique.
La dťmarche "Bidon Futť" ťtant en principe appliquťe tout au long de
l'annťe, ce T.P. peut nťanmoins Ítre rťalisť au moment jugť opportun par chacun.
Polycopiť distribuť aux ťlŤves:
Les 8 pages suivantes forment le polycopiť distribuť aux ťlŤves
(nous avons fait figurer en bleu les rťponses attendues dans
le cas d'expťriences rťussies). Il consiste en 2 feuilles A3 recto-verso pouvant
constituer, une fois pliťes, un livret format A3.
La 1ťre feuille (pages 3,4,9 et 10 ci-aprŤs) est distribuťe pendant le cours
prťcťdant la sťance de T.P. Les pages 3 et 4 sont exploitťes en faisant le point sur
la visite du pilote et exploitant les notes prises par les ťlŤves ŗ cette occasion.
La 2ťme feuille (pages 5,6,7 et 8) est distribuťe en dťbut de sťance de
T.P.
Les pages 9 et 10 sont exploitťes lors du cours suivant ("dťbriefing" du
T.P.). C'est l'occasion d'une sensibilisation des ťlŤves aux problŤmes
d'ťcotoxicologie et de long terme et de prťciser la notion de dťchet.
Rťactifs utilisťs:
Les solutions ioniques proposťes ici ne sont qu'indicatives, chaque
collŤgue ťtant libre d'adapter les compositions ŗ sa propre progression. Nous avions
retenu le test de dťcoloration d'une solution (K+ + MnO4-)
par le zinc en prťsence d'ions NO3- pour la mise en ťvidence des
nitrates et le cuivre pour le TP "ťlťments chimiques". Cela explique notre
choix.
Les concentrations indiquťes pour la solution ŗ traiter (voir la liste de produits et
matťriel) rťsultent d'un compromis entre :
- la nťcessitť d'avoir un g‚teau de filtration apprťciable et donc un volume de
prťcipitť suffisant
- le soucis d'ťviter la formation de MnO2 .
Le zinc est utilisť en poudre plutŰt qu'en grenaille afin de diminuer la durťe de la
premiŤre expťrience (aire spťcifique beaucoup plus favorable). Il permettra ťgalement
de visualiser le g‚teau de filtration sur le papier filtre quel que soit le volume de ce
g‚teau.
Prťcautions expťrimentales:
Expťrience 1: Traitement de la solution oxydante.
3 gouttes d'acide nitrique ŗ 50 % sont suffisantes pour une dťcoloration en moins de 5
minutes. Davantage d'acide demandera d'autant plus de soude pour neutraliser avant de
pouvoir prťcipiter les hydroxydes mťtalliques (expťrience 2).
Expťrience 2: Prťcipitation des hydroxydes mťtalliques.
Ajouter la soude ŗ la solution dťcantťe (ne pas agiter avant l’ajout de la soude)
afin de pouvoir visualiser l'apparition du prťcipitť blanc dans le surnageant (le
phťnomŤne serait moins visible avec la poudre de zinc en suspension).
Les hydroxydes mťtalliques obtenus ne se redissolvent qu'ŗ pH =14. Il est donc peu
probable de perdre du prťcipitť ainsi.
Expťrience 3: Filtration.
. S'il reste un peu de temps il peut Ítre intťressant de traiter le filtrat devant les
ťlŤves:
- ajout d'un peu de soude: on ne devrait en principe voir aucun prťcipitť d'hydroxyde
mťtallique
- il suffit alors de neutraliser la solution (mesure au papier pH par un ťlŤve) avec de
l'acide chlorhydrique (pour ťviter de rejeter des ions nitrate) avant de rejeter celle-ci
ŗ l'ťvier devant les ťlŤves.
Expťrience 4: Pluies acides.
La lixiviation est un peu lente. Si le temps presse il est possible de rť-utiliser les
fioles ŗ vide de l'expťrience 3 ŗ condition de les rincer soigneusement pour qu'il n'y
ait aucune ťquivoque sur la provenance du prťcipitť obtenu par ajout de soude au
lixiviat.
INTRODUCTION
Dans le cadre gťnťral de l'opťration "Bidon Futť", un tri sťlectif des dťchets chimiques issus des sťances de travaux pratiques a ťtť mis en place au Lycťe. Selon leur nature, ces dťchets sont stockťs dans des bidons de diffťrentes couleurs.Rappels:
1/ - Les bidons blancs contiennent un mťlange d'acides et de bases. Les solutions doivent Ítre neutralisťes (le pH doit Ítre ajustť ŗ une valeur voisine de 7 ) avant d'Ítre rejetťes ŗ l’ťgout. Cette opťration est effectuťe dans la cuve (C1) (possibilitť d’ajout automatique d'une solution acide ou d'une solution basique).
2/ - Les bidons bleus contiennent des cations mťtalliques. On effectue la prťcipitation de ces mťtaux sous forme d'hydroxydes. Cette opťration est effectuťe dans la cuve (C2). Les ions hydroxyde sont apportťs par une solution de lait de chaux ou hydroxyde de calcium ( Ca2+ + 2 HO- ). La solution est ensuite dťcantťe dans la cuve (D). Les boues obtenues sont ensuite filtrťes. Elles seront envoyťes , aprŤs une ťventuelle stabilisation en dťcharge contrŰlťe . Si les opťrations ont ťtť conduites correctement, le filtrat est alors purifiť de ses polluants. Il sera envoyť ŗ l’ťgout aprŤs vťrification et neutralisation.
3/ - Les bidons jaunes contiennent des oxydants. Il faut "dťbarrasser" la solution de ce caractŤre oxydant. On appelle cela une rťduction (la thťorie sera vue en classe de premiŤre). Cette opťration est rťalisťe dans la cuve (C1) (possibilitť d’ajout automatique d'une solution rťductrice) oý on ajuste ťgalement le pH pour optimiser la rťaction. La suite du traitement est alors similaire au paragraphe prťcťdent (cuves C2 et D).
Nous allons traiter dans le cadre de ce TP le contenu d'un bidon jaune (oxydants), car cela va nous permettre d'examiner plus en dťtail chacune des ťtapes dťcrites ci-dessus.1/ TRAITEMENT DE LA SOLUTION OXYDANTE:
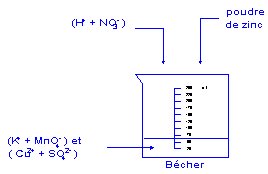
Prendre le petit bidon jaune disponible sur la paillasse. Lire le contenu sur l'ťtiquette renseignťes par les utilisateurs. Le bidon jaune contient: ( K+ + MnO4- ) et ( Cu2+ + SO42- ).1.1 MODE OPERATOIRE: Schťma: |
 |
- verser la moitiť du contenu du flacon jaune dans un bťcher.
- ajouter quelques gouttes d'acide nitrique concentrť ŗ l'aide du compte gouttes.
- ajouter une spatule de poudre de zinc (dťlicatement pour ťviter les projections ).
- agiter doucement
- laisser dťcanter quelques minutes
A quoi sert l'acide nitrique ? - ŗ obtenir un
pH acide
- ŗ fournir les ions nitrates (catalyseur)
1.2. OBSERVATIONS:
- dťcoloration du permanganate de potassium
- dťcoloration du sulfate de cuivre dont la couleur ťtait masquťe par celle du
permanganate de potassium.
1.3 INTERPRETATION:
- rťaction complexe de dťcoloration du
permanganate de potassium par le zinc en prťsence d'ions nitrate NO3-
(cf TP identification des ions)
- rťaction des ions Cu2+ avec le
zinc mťtal (Cu2+ + Zn ŗ Cu + Zn2+
) (cf TP sur l'ťlťment cuivre)
2. PRECIPITATION DES HYDROXYDES METALLIQUES
Pour l'ťtape de prťcipitation on utilise sur le pilote du lait de
chaux ( Ca2+ + 2 HO- ). Dans ce T.P. nous allons utiliser une
solution de soude.
Quel est le nom scientifique de la solution de soude ? Quelle est sa formule chimique?
solution d'hydroxyde de sodium ( Na+ + HO- )
Lait de chaux ou soude ne change rien au principe de l'opťration: il s'agit dans les deux cas d'apporter des ions hydroxyde.
2.1 MODE OPERATOIRE: Schťma: |
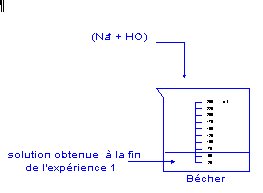 |
2.2 OBSERVATIONS:
Apparition d'un prťcipitť blanc (ou blanc-rose ) dans le surnageant qui se mťlange ŗ la poudre de zinc en suspension.
2.3 INTERPRETATION:rťaction de prťcipitation entre les cations
mťtalliques prťsents et les ions hydroxyde
Zn2+ + 2 HO- ŗ Zn(HO)2 (s)
prťcipitť de couleur blanche
Mn2+ + 2 HO- ŗ Mn(HO)2 (s) prťcipitť
de couleur blanc - rose
3. FILTRATION:
3.1 MODE OPERATOIRE: Schťma: |
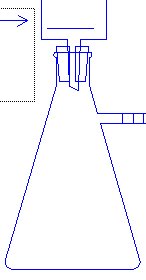 |
- placer le papier filtre sur le bŁchner., humidifier lťgŤrement le papier
filtre.
- mettre en route la trompe ŗ vide :
a/- ouvrir le robinet d'eau
b/- connecter le tuyau en caoutchouc ŗ la fiole ŗ vide (robinet d'aspiration en
position fermťe)
- mettre en suspension le prťcipitť en agitant un peu
- verser le contenu du becher sur le filtre, observer.
- ouvrir le robinet d'aspiration de la trompe ŗ vide, observer.
- quand la filtration est achevťe, fermer le robinet d'aspiration, dťconnecter le tuyau
en caoutchouc puis fermer le robinet d'eau.
Le filtrat sera rťcupťrť dans un bidon spťcial pour vťrification et ťventuel traitement complťmentaire par le professeur avant rejet ŗ l’ťgout.
3.2 OBSERVATIONS:
- on rťcupŤre un filtrat
incolore
- la filtration est beaucoup plus facile avec le robinet d'aspiration ouvert.
- on obtient un g‚teau gris foncť.
3.3 INTERPRETATION:
- Les prťcipitťs (blancs)sont retenus par le
papier filtre de mÍme que la poudre de zinc (noire)
ū on obtient un g‚teau de filtration gris foncť.
- La filtration est facilitťe lorsque la fiole est "sous vide". En fait, comme on crťe une dťpression dans la fiole (c.a.d. que l'on y fait rťgner une pression infťrieure ŗ la pression atmosphťrique), c'est la pression atmosphťrique qui "pousse" le liquide ŗ travers le g‚teau de filtration.
4. SIMULATION DE L'ACTION DES PLUIES ACIDES:
Les g‚teaux de filtration peuvent ( et doivent) Ítre stockťs
dans des dťcharges spťcialisťes. MÍme enterrťs ces dťchets seront soumis ŗ l'action
des eaux de pluies (rappelons-nous du lessivage dans le cycle de l'azote). La situation
est mÍme aggravťe quand les eaux de pluie sont acides, ce qui est malheureusement assez
frťquent aujourd'hui.
Citer un corps responsable des pluies acides ? le dioxyde d'azote
NO2 (voir le cycle de l'azote )
Nous allons simuler l'action de ces pluies acides sur les g‚teaux stockťs en
dťcharge en faisant percoler une solution acide ŗ travers le g‚teau.
Remarque: En gťnťral les pluies acides sont moins acides que la solution utilisťe. Nous
utilisons celle-ci pour accentuer les rťsultats.
4.1 MODE OPERATOIRE: Schťma: |
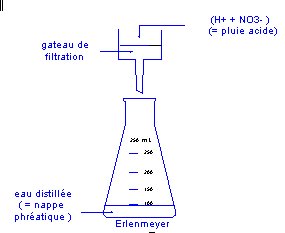 |
- mettre un fond d'eau distillťe dans l'erlenmeyer ( pour
simuler la nappe phrťatique )
- verser un peu de solution d'acide nitrique sur le g‚teau toujours en place sur le
bŁchner
- ŗ la fin de l'opťration ajouter quelques gouttes de soude au contenu de l'erlenmeyer.
Observer.
- effectuer la mÍme opťration dans un tube ŗ essai tťmoin contenant un peu de solution
acide. Observer.
A la fin de l'opťration placer les g‚teaux de filtration dans la poubelle idoine et
vider les fioles ŗ vide dans le bidon futť appropriť. Lequel ?
Bidon bleu (mťtaux)
4.2 OBSERVATIONS:
Le liquide rťcupťrť dans l'erlenmeyer est
incolore
On observe la formation d'un prťcipitť dans la fiole ŗ vide mais pas dans le tube ŗ
essais.
4.3 INTERPRETATIONS:
Nous avons mis en ťvidence la prťsence de
cations mťtalliques dans la fiole ŗ vide (ici des ions Zn2+
et des ions Mn2+ )Une fraction du g‚teau s'est donc redissoute par
ajout d'acide.
Le mÍme phťnomŤne ŗ dťjŗ ťtť constatť lors du TP test d'identification
des ions. Donner un exemple:
redissolution du prťcipitť d'hydroxyde de baryum par ajout
d'acide.
5. CONCLUSION:
Des traitements chimiques permettent de dťbarrasser les solutions de
leur caractŤre oxydant, dangereux pour les cellules des organismes vivants (cf.
expťrience 1).
D'autres traitements permettent d'ťliminer les ions mťtalliques des eaux ŗ purifier.
Ainsi la prťcipitation permet de passer d'ions mťtalliques aqueux, difficilement
isolables, ŗ des prťcipitťs d'hydroxydes mťtalliques (cf. expťrience 2), donc solides
et facilement sťparables par dťcantation et par filtration (cf. expťrience 3). Ce
procťdť est couramment utilisť dans les stations de traitement d'eau.
Si les dťchets chimiques solides (p.e. dťchets de TP, certaines boues de stations
d'ťpuration, cendres d'incinťrateurs ...) sont placťs sans prťcaution dans une
dťcharge, l'eau de pluie peut provoquer une dissolution partielle de certains composťs
et entraÓner ceux-ci vers la nappe phrťatique. On appelle ce phťnomŤne la lixiviation
(cf. expťrience 4).
(Voir en annexe ŗ titre indicatif les effets ťcotoxicologiques du sulfate de cuivre et du sulfate de zinc)
Pour ťviter ce problŤme on procŤde ŗ des tests de lixiviation sur les dťchets afin de dťterminer si ceux-ci doivent Ítre stabilisťs (enrobage ŗ l'aide de matiŤres inertes). Si leur composition le justifie, ils sont ensuite stockťs dans des dťcharges spťciales dites "dťcharges contrŰlťes". Celles-ci sont situťes sur des sites gťologiques particuliers oý une couche impermťable du sous-sol permet de protťger les nappes phrťatiques. Elles sont par ailleurs ťquipťes d'un systŤme de captage des eaux de ruissellement.
"Nous ne sommes pas les
propriťtaires de la planŤte sur laquelle nous vivons,
nous n'en sommes que les gťrants "
(Commandant Jacques Yves Cousteau).
EFFETS ECOTOXICOLOGIQUES DU SULFATE DE ZINC : ( Zn2+ + SO42- )
Concentration dans l'eau |
effet |
pťriode lťtale |
10 mg.L-1 |
truites |
30 h |
0.6 mg.L-1 |
jeunes saumons |
30 h |
1.5 mg.L-1 |
ťpinoches |
24 h |
0.4 mg.L-1 |
ťpinoches |
7 jours |
Pťriode lťtale: laps de temps durant lequel les poissons sous essai
subissent des lťsions telles que le fait de les remettre dans l'eau fraÓche ne les
empÍchera plus de mourir.
La dose lťtale est d'autant plus faible que la pťriode d'exposition est longue.
Les effets ŗ trŤs long terme d'exposition ŗ des concentrations trŤs faibles sont
encore mal connus.
EFFETS ECOTOXICOLOGIQUES DU SULFATE DE CUIVRE : ( Cu2+ + SO42- )
EspŤces animales ou vťgťtales |
Concentration lťtale au bout de 4 jours |
certaines algues |
0.1 ŗ 0.5 mg.L-1 |
daphnies |
1 mg.L-1 |
Carpes |
0.35 mg.L-1 |
Saumons adultes |
0.1 mg.L-1 |
Jeunes saumons |
0.05 mg.L-1 |
Lorsque sulfate de cuivre et sulfate de zinc sont mťlangťs, leurs effets toxiques sont multipliťs plusieurs fois !!!
ū Cela doit vous faire rťflťchir sur les effets ťcotoxicologiques du lixiviat obtenu dans la partie nį 4 du T.P.!!!
( source: Les eaux industrielles rťsiduaires. Meinck, Stooff et KohlschŁtter. Masson ťditeur )
LISTE DE MATERIEL
PREVOIR POUR CHAQUE BINOME:
- 1 fiole ŗ vide 500 ml avec potence, noix et pince
- 1 bŁchner avec papier filtre
- 1 trompe ŗ vide (1 par paillasse suffit)
- 1 bťcher de 250 ml
- 1 bťcher de 50 ml
- 1 agitateur en verre
- 1 ťprouvette graduťe de 25 ml
- 1 erlenmeyer de 250 ml
- 1 spatule
- 1 pissette d'eau distillťe
- 1 tube ŗ essai avec porte-tubes
- du papier essuie-tout
- acide nitrique 50 % en flacon compte-gouttes
- acide nitrique 0.1 M
- soude 5 M en flacon compte-gouttes
- poudre de zinc
- 1 flacon jaune contenant 100 ml (50 ml pour chaque groupe) d'une solution 0.01 M de
permanganate de potassium et 0.1 M de sulfate de cuivre.
POUR L'ENSEMBLE DE LA CLASSE:
- 1 bidon futť bleu
- 1 bidon futť jaune
- 1 bidon futť blanc
- 1 poubelle pour les g‚teaux de filtration
- 1 flacon de lait de chaux et d'eau de chaux (pour montrer aux ťlŤves)
![]() Pour Tťlťcharger le TP (zip 64 ko) (word6)
Pour Tťlťcharger le TP (zip 64 ko) (word6)
| |