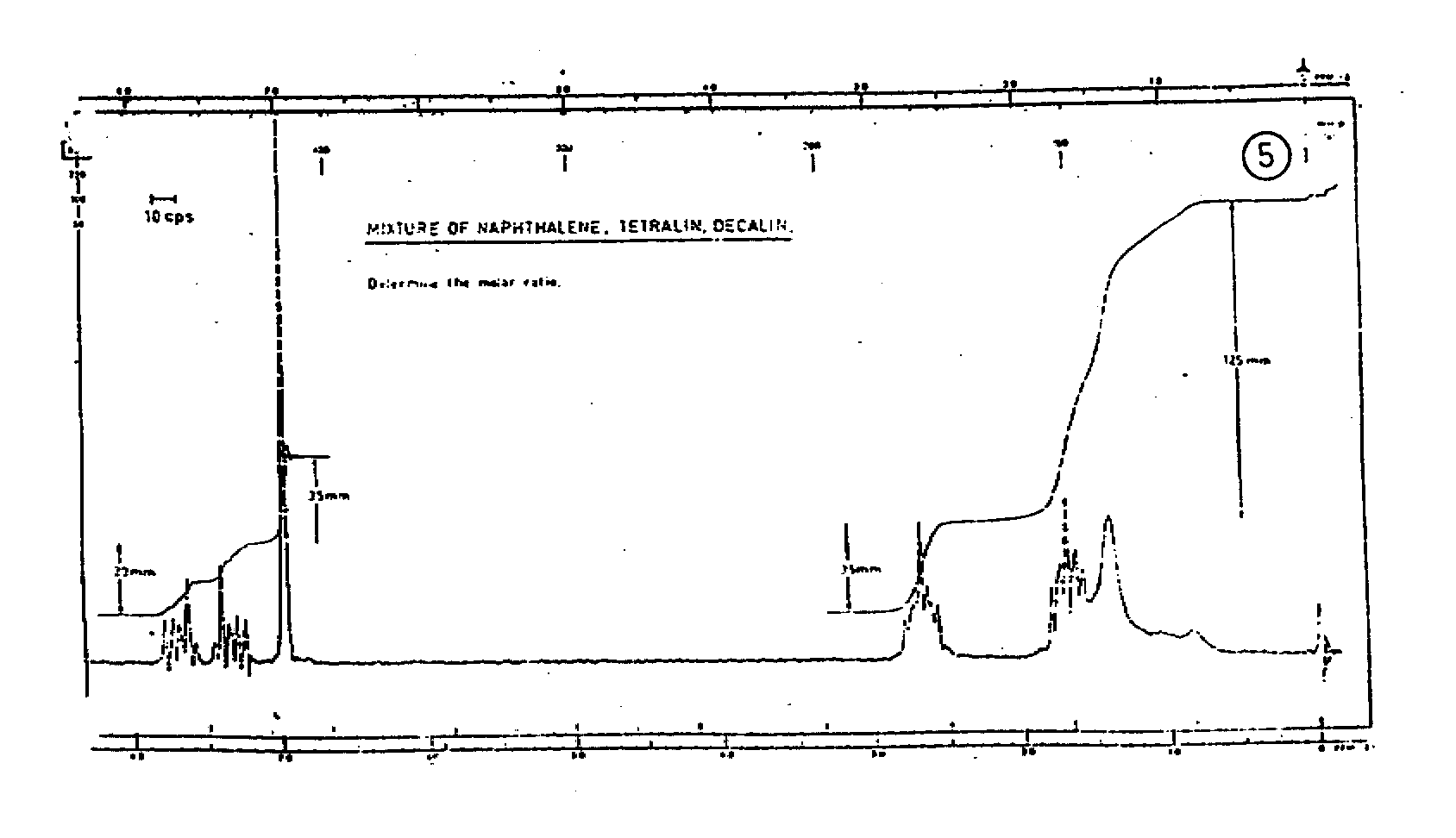
1. Pour qu’un composé soit aromatique, il faut et il suffit que son système p contienne 4n + 2 électrons. Les systèmes suivants sont-ils aromatiques ? ![]()
2. Écrire les formes mésomères et donner la structure électronique réelle des molécules suivantes :
- propènonitrile CH2 = CH – CN
- paraméthoxynitrobenzène
3. Comparer l’acidité des composés suivants :
3.1. paraméthylphénol paranitrophénol métanitrophénol phénol
3.2. acide benzoïque acide paraméthoxybenzoïque acide métaméthoxybenzoïque
3.3. ion anilinium ion o,o-diméthylanilinium ion m-fluoroanilinium
3.4. acide phénylacétique acide paraméthoxy phénylacétique.
4. Quelles sont les positions de la pyridine 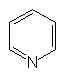 qui sont les plus sensibles
qui sont les plus sensibles
aux attaques nucléophiles ?
aux attaques électrophiles ?
Mêmes questions pour le thiophène 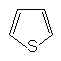
5. Écrire les formes mésomères de l’anion cyclopentadiènyle.
6. Classer par ordre de stabilité croissante les cations suivants :
6.1. diphénylméthyle 6.2. diméthylméthyle 6.3. éthènyle
6.4. prop-2-èn-1-yle 6.5. éthyle 6.6 phénylméthyle
6.7. paraméthoxyphénylméthyle
7. Les réactions de substitution électrophile ont été décrites succintement en cours. Tracer un diagramme donnant l’énergie du système en fonction du degré d’avancement de la réaction (x).
8. Comment l’électrophile E+ est-il formé dans les réactions suivantes :
8.1. nitration des composés aromatiques réactifs par HNO3 sans catalyseur.
8.2. nitration du benzène par le mélange HNO3 – H2SO4.
8.3. Chloration par HOCl en présence de HCl comme catalyseur.
8.4. Nitrosation (introduction d’un groupe – NO ) de dérivés aromatiques réactifs par de l’acide nitreux HNO2 en milieu acide fort.
9. Comparer les effets activants des groupes ortho / para – directeurs suivants :
9.1. – OH 9.3. – O – 9.5. –O – CO – CH3
9.2 – NH2 9.4. – NH – CO – CH3
10. Expliquer le fait suivant :
La nitration du tertiobutylbenzène ne fournit que 16% de produit
11. On peut utiliser le nitrobenzène mais non le benzène comme solvant lors de l’alkylation de Friedel et Crafts du bromobenzène. Expliquer.
12. Écrire l’équation équilibrée de la substitution du paraxylène (1,4-diméthylbenzène) par le brome et tracer un diagramme donnant l’enthalpie DH de la réaction en fonction de l’avancement de la réaction x . Si on ajoute un catalyseur à base de fer au mélange, la substitution est grandement accélérée. Quelles modifications cela entraîne-t-il dans le diagramme énergétique ?
13. Indiquer par une flèche quelles sont les positions des composés suivants qui sont les plus susceptibles de subir les substitutions électrophiles :
13.1.méta-xylène 13.2. paranitrotoluène 13.3. méthyl-1 phénol
13.4 métachloronitrobenzène 13.5. paraméthoxytoluène
13.6. parachlorotoluène 13.7. métanitrotoluène
13.8. métafluorotoluène 13.9. méta-éthyl-biphényle
13.10. para chloro-acétanilide
14. Quel est celui des 3 xylènes qui est sulfoné le plus facilement ?
15. Expliquer le fait suivant : De tous les halogénures d’aryle, le fluorobenzène est celui qui fournit le moins de dérivé " ortho ".
16. On isole du pétrole un liquide incolore et volatil. Le spectre IR de ce composé comporte un pic de forte intensité à 3020 cm–1 , un pic d’intensité moyenne à 2910 cm–1 , un pic important à 1490 cm–1 , un pic intense à 730 cm–1 et un autre à 690 cm–1 . Le spectre RMN se compose de deux singulets à 2,32 ppm et 7,17 ppm, qui s’intègrent dans le rapport 1/1,65 respectivement. L’analyse centésimale révèle la présence de 91,3% de carbone et de 8,7% d’hydrogène. Quelle est la structure de ce composé ?
17. Donner les produits des réactions suivantes. Indiquer dans chaque cas si la réaction est plus lente ou plus rapide qu’avec le benzène .
17.1 ![]() 17.2.
17.2. ![]()
17.3 ![]() 17.4.
17.4. ![]()
17.5. ![]() 17.6
17.6 ![]()
17.7. ![]() 17.8.
17.8. ![]()
18. Proposer un mécanisme pour la réaction :
Acide paratoluènesulfonique
![]() toluène + acide sulfurique
toluène + acide sulfurique
19. Préparer à partir du phénol l’acide 2-hydroxy-5-nitro-benzoïque
20. Qu’obtient-on par nitration du 1-nitro-4-éthanoyl-naphtalène ?
21. Compléter les réactions
21.1.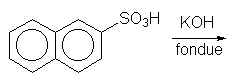
21.2.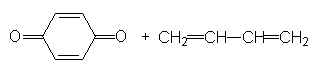
22. Un composé " A " de structure inconnue a pour formule brute C9H10 . Combien comporte-t-il de sites d’insaturation ? Son spectre RMN présente un singulet (3p) à 2,3 ppm, un multiplet (3p) vers 5 ppm et un multiplet (4p) à 7 ppm. Quand on traite " A " par l’ozone en faible concentration, puis par du zinc en milieu acétique, on isole " B " qui a le spectre RMN suivant : singulet (3p) à 2,3 ppm, multiplet (4p) à 7,2 ppm, et singulet (1p) à 9,5 ppm. Quand " B " est oxydé par le permanganate de potassium aqueux à chaud, un autre composé " C " est isolé, de formule C8H6O4 , dont le spectre RMN est ainsi constitué : multiplet (4p) à 7,4 ppm et singulet (2p) à 12 ppm. Par chauffage avec P2O5 , " C " conduit à l’anhydride phtalique . Quelles sont les structures de " A " , " B " , et " C " .
23. Un composé " A " C4H4O3 présentant en RMN un singulet à 2,7 ppm uniquement, réagit avec un composé " B " comportant 77,8% de carbone, 7,4% \ d’hydrogène et 14,8% d’oxygène. Cette réaction se fait en présence de AlCl3 anhydre, à raison de 2,2 moles pour une mole de " A ". Expliquer ce phénomène et dire de quelle réaction il s’agit. Le produit obtenu après hydrolyse (" C ") comporte 63,5% de carbone, 5,8% d’hydrogène et 30,7% d’oxygène. On traite " C " par du zinc amalgamé en présence d’acide chlorhydrique, pour obtenir " D " , lui même soumis à l’action de H3PO4 pur. On obtient " E ", que l’on traite par un mélange d’hydrazine et de potasse dans le diéthylène glycol. Le spectre RMN du produit obtenu se présente ainsi :
|
déplacement chimique |
1,3 |
2,4 |
4,2 |
7 – 8 |
|
forme du multiplet |
triplet |
triplet |
singulet |
massif |
|
rapports d’intégration |
1,33 |
1,33 |
1 |
1 |
Le spectre IR présente 4 bandes intéressantes :
à 1605 cm–1 (moyenne)
à 1495 cm–1 (moyenne)
à 880 cm–1 (intense)
à 710 cm–1 (très faible)
Déterminer " A ", " B ", " C ", " D ", " E ", " F " que l’on nommera.
24. Déterminer le pourcentage de naphtalène, tétraline et décaline du mélange dont on donne le spectre RMN ( voir feuille ci-jointe )