Cinétique électrochimique - Tracé de courbes intensité-potentiel |
1. Tracé des courbes intensité
potentiel des systèmes :
2H+aq + 2 e- ® H2 et 2H2O® O2 + 4H+aq + 4 e-
|
Montage
à trois électrodes
Solution d'acide sulfurique |
R :
électrode de référence (E.C.S.) T :
électrode de travail (celle que l'on veut étudier ) A :
électrode auxiliaire ( Pt ou inox ) |
Mise
en évidence des surtensions.
Variantes
:
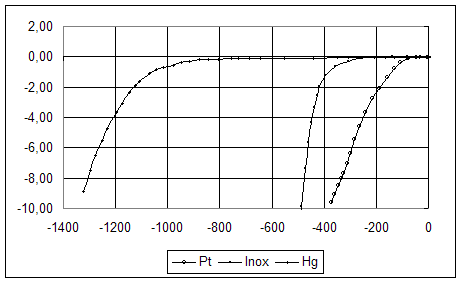
·
Influence de la nature de la cathode
sur la valeur de la surtension (cathode en Pt, inox, Hg).
Solution
d'acide sulfurique
2. Application : Electrolyse d'une
solution d'acide sulfurique. Tension minimale à appliquer.
Utiliser
le même montage que ci-dessus en supprimant l'électrode de référence.
3. Vagues d’oxydation de métaux
(électrolyte = solution molaire de chlorure de sodium)
|
|
|
|
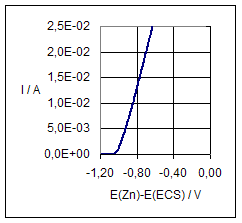
Vague
d’oxydation du zinc |
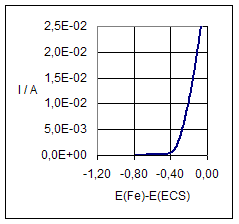
Vague
d’oxydation du fer |
Expériences
réalisées à l’aide du potentiostat RADIOMETER PGP201.
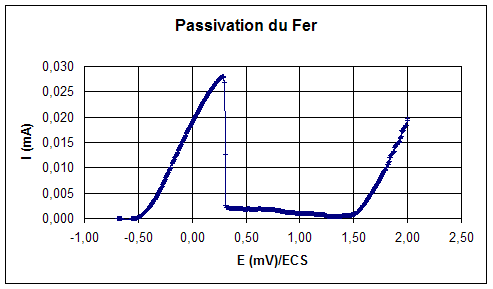
4. Passivation du fer
---------------------------------------------
Page d’accueil Pages « avancement d’une réaction électrochimique » Pages chimie