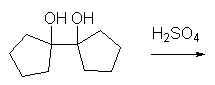
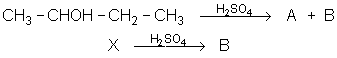1. Écrire les formules des composés suivants :
|
pentan-2-ol |
octan-2-ol |
3-méthyl hexan-1-ol |
3,3-diméthyl heptan-2-ol |
|
butan-1,4-diol |
cyclohexanol |
2-méthyl cyclohexanol |
3,4-diméthyl cyclohexanol |
2. Compléter les réactions suivantes :
|
2-méthyl
butan-2-ol |
hexan-2-ol |
pentan-1-ol |
|
propan-1-ol |
butan-2-ol |
éthanol |
|
propan-2-ol |
butan-2-ol
|
pentan-1-ol
|
3. Indiquer les réactifs permettant d’effectuer les synthèses suivantes :
|
propan-1-ol ¾ ® CH3CH2CH2
– O – CH(CH3)2 |
hexan-1-ol ¾ ® hexan-2-one |
|
pentan-1-ol ¾ ® pent-1-yne |
1-bromo propane ¾ ® 2-méthyl pentan-2-ol |
|
butan-2-ol ¾ ® 3,4-diméthyl hexane |
pentan-2-ol ¾ ® ….. + C6H6 ¾ ® 2-phényl pentane |
|
2-méthyl phénol ¾ ® heptan-1,6-diol |
|
4. Un composé A a pour formule C5H12O. A est optiquement actif. Les vapeurs de A après passage sur alumine (Al2O3) donnent un composé B. B réagit avec Br2 pour donner C. D’autre part B donne, par action de l’ozone puis traitement, du propanal et de l’éthanal. Déterminer A, B et C.
5. Compléter les réactions suivantes :
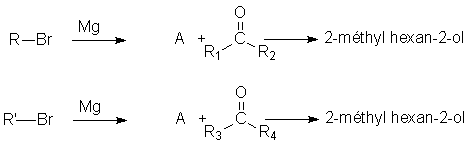
6. Qu' obtient-on dans les réactions suivantes ?

7.Comment peut-on effectuer les réactions suivantes :
(R) Butan-2-ol ¾ ¾ ® (R) 2-chlorobutane
(R) Butan-2-ol ¾ ¾ ® (S) 2-chlorobutane
8.Décrire sommairement le mécanisme de la réaction suivante :
Butan-1-ol + HBr ![]() 1-bromobutane + H2O
1-bromobutane + H2O
Tracer le diagramme de réaction
Quelle est l’expression de la vitesse
Mêmes questions pour la réaction suivante :
2-méthylbutan-2-ol + HBr ![]() 2-bromo-2-méthylbutane + H2O
2-bromo-2-méthylbutane + H2O
9. La substitution de — OH par — Br peut se faire par réaction d’un alcool sur le bromure d’hydrogène. Il y a d’abord attaque électrophile de O par H+ , puis départ de H2O , et attaque du cation formé par Br– .
9.1.Écrire le mécanisme de cette réaction SN1 dans le cas général.
9.2. Chacun des énantiomères unlike du 3-bromo-butan-2-ol donne le méso–2,3-dibromo-butane par action de HBr. Expliquer la stéréochimie de cette réaction.
10. Les alcools ne réagissent pas avec NaBr, mais l’addition de H2SO4 conduit aux halogénures d’alkyle. Expliquer.
11.Un composé « A » réagit avec HIO4 pour donner un seul composé « B ». Ce dernier présente une forte bande d’absorption IR à 1720 cm–1 . Le composé « A » , traité par H2SO4 concentré, donne un composé « C » de formule C6H12O . Le spectre de RMN de « C » ne montre que deux singulets : d = 1,10 ppm (9 H) et d = 2,05 ppm (3 H). Quelles sont les structures de « A » , « B » et « C » ?
12. Compléter les réactions ci-dessous :
12.1. 3,3-dichloroprop-1-ène + C2H5O– ¾ ¾ ®
12.2. 2-méthylpropan-2-ol +
méthanol ![]()
12.3. 2-méthylbutan-1-ol + HBr ¾ ¾ ®
12.4. 2-méthylbutan-1-ol + PBr3 ¾ ¾ ®
12.5. 3-bromoéthoxybenzène +
HI ![]()
12.7. 5-bromopentan-1-ol + ![]() ¾ ¾ ®
¾ ¾ ®
13. Comment pourrait-on effectuer les transformations suivantes ? (plusieurs étapes peuvent être nécessaires).
13.1. 2-méthylcyclopentanol ¾ ¾ ® 1-méthylcyclopentanol
13.2. 1-méthylcyclopentanol ¾ ¾ ® 2-méthylcyclopentanol
13.3. But-1-yne + éthanol ¾ ¾ ® hexan-3-one
14. Une tentative de préparation du tertiobutyléthène, par chauffage du tertiobutyléthanol (ou 3,3-diméthylbutan-2-ol) avec de l’acide sulfurique, a fourni en fait une oléfine de formule attendue C6H12 , mais dont les propriétés physiques et spectroscopiques sont différentes de celles du tertiobutyléthène. Expliquer ce qui s'est passé.
15.
Le composé « A » ( R = C2H5 ), par traitement
acide, donne « B » et « C » .
Indiquer toutes les étapes de ces transformations.
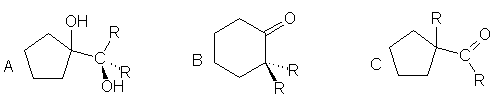
Si R = C6H5 , « A » donne seulement B. Expliquer pourquoi .
16. Un composé « C », qui est un anesthésique 7 fois plus puissant que l’éther, est préparé‚ à partir de l’éthylène de la manière suivante :
![]()
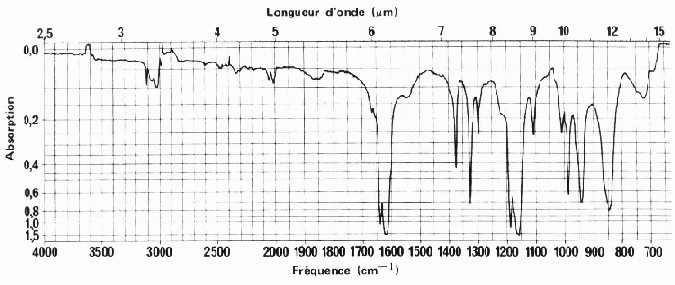
On donne les spectres RMN et IR de C. (voir feuille ci-jointe) Interpréter les spectres.Quelles sont les structures des composés « A » , « B » et « C » ?

17. Donner le produit obtenu dans la transposition pinacolique suivante :
1-parabromophényl-1,2-diphényl-2-paraméthoxyphényléthane-1,2-diol + H2SO4
18. Comment synthétiser le 2,3,3-triméthylbutan-2-ol à partir de propanol et de méthanol ?
19. Par hydrolyse totale de 8,2 g d'un composé « A », on a obtenu 6,1 g d’un corps « B » et un monoacide carboxylique « D ». 0,3 g de « D » sont exactement neutralisés par 5 cm3 d’une solution de soude M . « B » est dédoublable. Par déshydratation, il donne E qui, sous l’action d’une solution concentrée de permanganate de potassium, conduit à l’acide benzoïque. Indiquer la formule structurale probable de « A » , « B » , « D » et « E »
20.
Compléter la suite de réactions suivante, en
explicitant succintement les réactions qui ont lieu. Remplacer les formules
brutes par les formules développées.

33.
Compléter les réactions suivantes :